Щавлева кислота: сучасні методи отримання та використання у промисловості
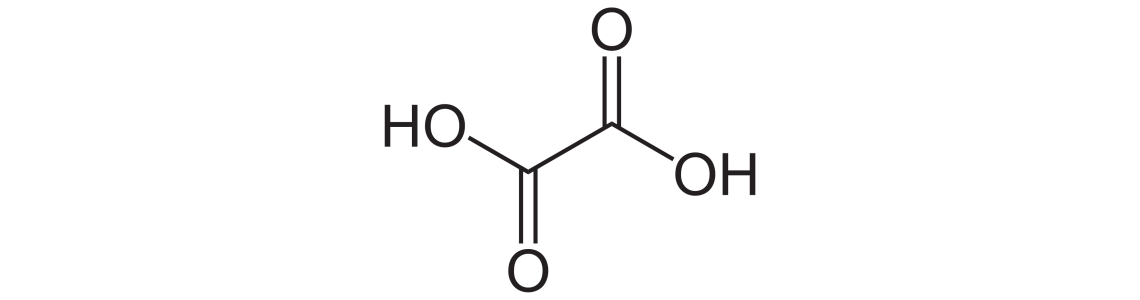

Що таке щавлева кислота? Іншими словами її ще називають етандіовою кислотою – це представник ряду 2-основних граничних карбонових кислот. У даному гомологічному ряду це найперший і найпростіший компонент.
Властивості та характеристики щавлевої кислоти
У природних умовах ця кислота може міститися у ревені, шпинаті, щавлі, карамболі, бегонії, тощо. В їхніх клітинах містяться частіше лише похідні кислоти – складні ефіри та солі щавлевої кислоти, що мають назву оксалати. Вони зустрічаються і в організмі людини, накопичуючись у сечовивідних шляхах, нирках і суглобах. Ці оксалати лікарі називають каміннями.
Цей хімікат має вигляд субстанції порошкоподібного типу, яка складається із дрібних кристалів білого кольору. Вони позбавлені виразного запаху й добре розчиняються у воді, спиртах, гліцерині, диметиловому ефірі, мурашиній кислоті, диметилсульфоксиді та фтороводневі. Зовсім не розчиняються кристали щавлевої кислоти в хлороформі, петролейному ефірі, бензолі, аміаку.
Щодо щільності самої речовини, то вона дорівнює 1,36 г / м³, тобто щавлева кислота на 36% важить більше, ніж вода.
Етандіова кислота одна з найсильніших у своєму підряді, тому в будь-яких хімічних взаємодіях вона підвищено активна. Наприклад, у результаті реакції окислення вона легко розпадається на воду та вуглекислоту. При нагріванні щавлева кислота розпадається на окис вуглецю, воду та вуглекислоту, особливо, якщо в якості каталізатора використовується концентрована сірчана кислота.
Варто відзначити, що цей хімікат дуже токсичний та вогненебезпечний. Недопустимо його попадання всередину організму навіть у мінімальній кількості, адже смертельна доза для людини складає менше 200 мг/кг маси тіла. У випадку попадання кислоти на слизові оболонки та шкіру відбувається сильна алергічна реакція, з’являються опіки. Небезпечно також вдихати її пил, він ще й створює підвищену пожежонебезпеку в приміщенні. Тому на складах недопустимо зберігати поруч із щавлевою кислотою сильні окислювачі, а також проводити роботи з вогнем.
Промисловий варіант отримання щавлевої кислоти
Технології синтезу хімікату діляться на дві групи:
- Перша базується на синтезі за допомогою окислювальних процесів, під час них різні види сировини піддають дії кислот, солей, кисню та інших реагентів. У якості сировини використовують вуглеводи, відходи дерева та сільського господарства, сланцеве та кам’яне вугілля, а також торф. В інших циклах виробництва застосовують відходи від цукрової промисловості, олефіни, етиленгліколь та інші види натуральної сировини. Як каталізатори застосовують сполуки марганцю, молібдену, ванадію, оксиди азоту та кисень.
- Другу групу складають технології, пов’язані з синтезом щавлевої кислоти та окису вуглецю. Вони менш затребувані, ніж попередній варіант, але ця технологія має більші перспективи для розвитку в майбутньому. На першій стадії синтезу з окису або двоокису вуглецю мурашинокислих солей, а потім їх трансформують в оксалати. Далі вони використовуються, як окрема сировина, або проходять через реакцію відновлення задля отримання безпосередньо щавлевої кислоти.
Сфери застосування щавлевої кислоти
Хімічна речовина має найширшу сферу застосування у виробництві. Перш за все, щавлева кислота – затребуваний реактив у багатьох напрямках аналітичної хімії. З нею пов'язаний синтез йодоводню, сполук на основі хлору.
Крім цього, щавлеву кислоту використовують в гальванотехніці, щоб в анодних ваннах осаджувати покриття з олова, алюмінію та свинцю, які необхідні для різних конструкційних елементів. З її допомогою проводиться осадження рідкоземельних металів із їх розчинів і інших рідин технічного типу. Здатність цієї кислоти розчиняти оксидні плівки та корозійні нашарування на металевих поверхнях важлива для її включення у склад очищувальних засобів виробничого призначення.
У бджільництві реактив широко застосовується для профілактики та лікування бджіл від ураження кліщем Варроа. У цьому варіанті щавлеву кислоту використовують методами:
- Сублімації – для боротьби з кліщем застосовують випарник щавлевої кислоти. Це спеціальний інструмент, за допомогою якого комах обробляють парами речовини при певній температурі з метою знищення шкідників.
- Обприскування – пасіки обробляють 2% -вим водним розчином.
Хімікат у процесі виготовлення чорнил і лакофарбової продукції. Щавлева кислота використовується при виробництві піротехнічних речовин, миючих та дезінфікуючих засобів побутового призначення, а також у металургії та деревообробці.
Варто відзначити, що діетиловий ефір щавлевої кислоти – це популярна протикорозійна присадка до паливно-мастильних матеріалів. Вона використовується як засіб протруєння сировини, яка в подальшому використовується у текстильному та шкіряному виробництві.
Диметиловий ефір щавлевої кислоти активно застосовується косметичною промисловістю в якості хелатного компоненту. Він проміжний продукт у синтезі великої групи хімічних сполук.
У чистому вигляді хімічна сполука в медичній галузі не використовується, але входить до складу лікарських препаратів від онкології. Щавлева кислота допомагає лікувати злоякісні ракові пухлини шляхом їхнього закислення, але разом із тим ніяк не пошкоджує роботу здорових клітин організму.
Раніше ми вже згадували про те, що етандіова кислота зустрічається в багатьох продуктах харчування рослинного походження. Щодо її кількісного вмісту в них із розрахунку на 100 г продукту:
- спаржа – 0,13 г;
- квасоля – 0,36 г;
- листя буряка – 0,61 г;
- капуста – 0,1 г;
- морква- 0,5 г;
- часник – 1,48 г;
- листя салату – 0,33 г;
- петрушка – 1,7 г;
- листя ревеню – 0,52 г;
- шпинат – 0,97 г.








