Щавелевая кислота: современные методы получения и использования в промышленности
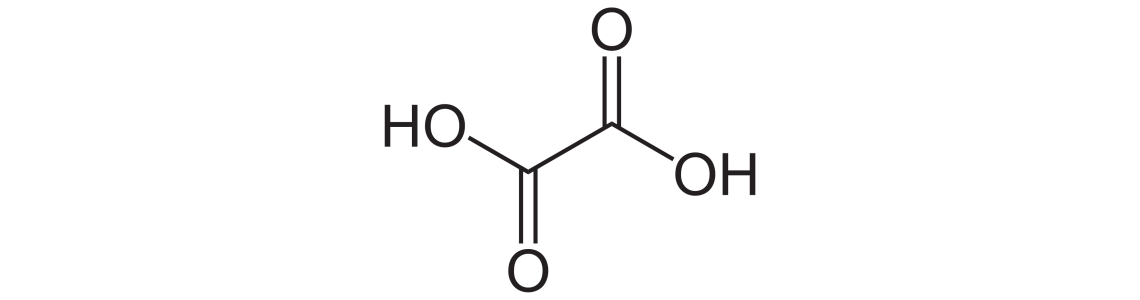
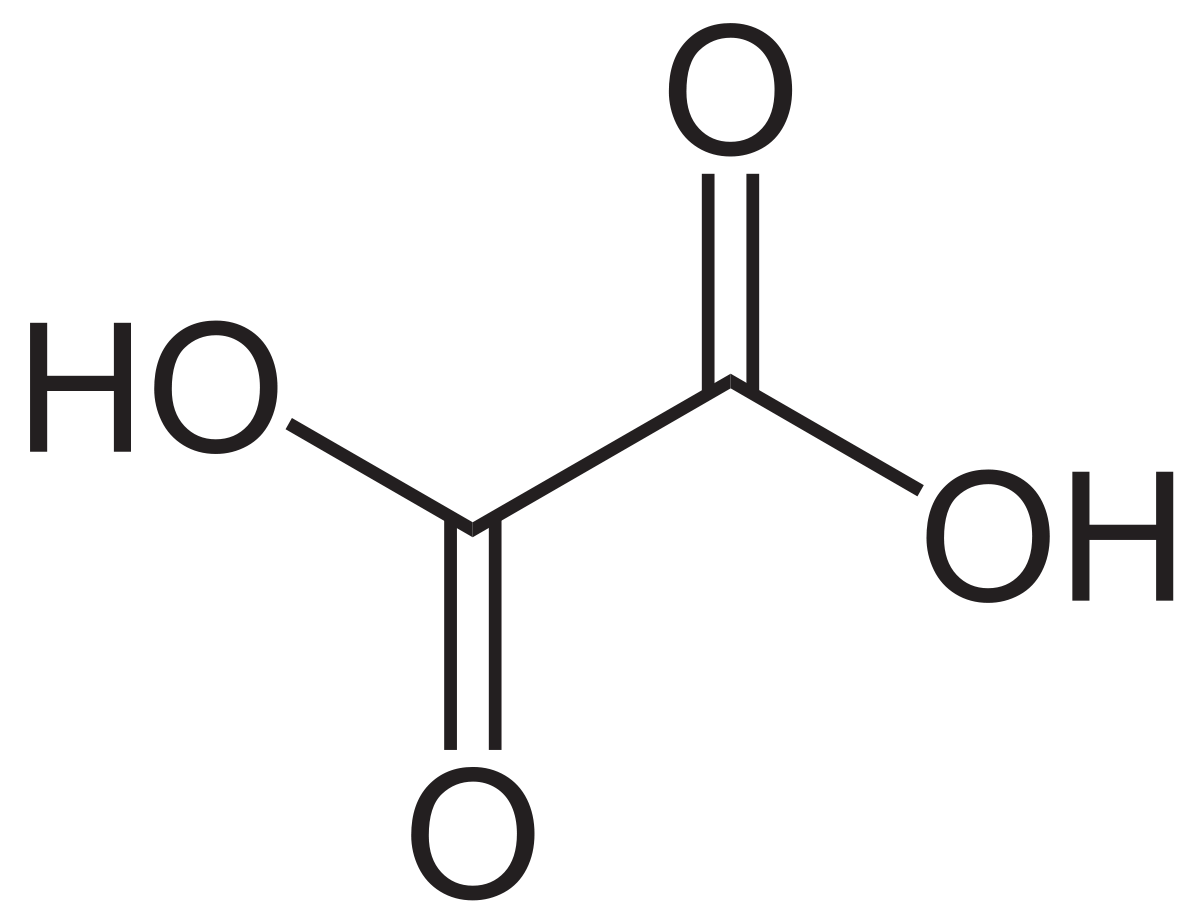
Что такое щавелевая кислота? Другими словами ее еще называют этандиовой кислотой – это представитель ряда 2-основных граничных карбоновых кислот. В данном гомологическом ряду это самый первый и простой компонент.
Свойства и характеристики щавелевой кислоты
В естественных условиях кислота может содержаться в ревене, шпинате, щавеле, карамболе, бегонии и т. д. В их клетках содержатся чаще производные кислоты – сложные эфиры и соли щавелевой кислоты, которые называются оксалаты. Они встречаются и в организме человека, накапливаясь в мочевыводящих путях, почках и суставах. Эти оксалаты врачи называют камнями.
Химикат представляет собой субстанцию порошкообразного типа, состоящую из мелких кристаллов белого цвета. Они лишены отчетливого запаха и хорошо растворяются в воде, спиртах, глицерине, диметиловом эфире, муравьиной кислоте, диметилсульфоксиде и фтороводородном. Совершенно не растворяются кристаллы щавелевой кислоты в хлороформе, петролейном эфире, бензоле, аммиаке.
Что касается плотности самого вещества, то она равна 1,36 г/м³, то есть щавелевая кислота на 36% тяжелее воды.
Этандиовая кислота одна из сильнейших в своем подряде, поэтому в любых химических взаимодействиях она повышена активна. К примеру, в результате реакции окисления легко распадается на воду и углекислоту. При нагревании щавелевая кислота распадается на окись углерода, воду и углекислоту, особенно если в качестве катализатора используется концентрированная серная кислота.
Следует отметить, что химикат токсичен и огнеопасен. Недопустимо его проникновение внутрь организма даже в минимальном количестве, ведь смертельная доза для человека составляет менее 200 мг/кг массы тела. В случае попадания кислоты на слизистые и кожу происходит сильная аллергическая реакция, появляются ожоги. Опасно также вдыхать ее пыль, она еще и создает повышенную пожароопасность в помещении. Поэтому на складах недопустимо хранить рядом со щавелевой кислотой сильные окислители, а также производить работы с огнем.
Промышленный вариант получения щавелевой кислоты
Технологии синтеза химиката делятся на две группы:
- Первая базируется на синтезе с помощью окислительных процессов, когда разные виды сырья подвергают действию кислот, солей, кислорода и других реагентов. В качестве сырья используют углеводы, отходы дерева и сельского хозяйства, сланцевый и каменный уголь, а также торф. В других циклах производства применяют отходы от сахарной промышленности, олефины, этиленгликоля и другие виды натурального сырья. В качестве катализаторов используют соединения марганца, молибдена, ванадия, оксиды азота и кислород.
- Вторую группу составляют технологии, связанные с синтезом щавелевой кислоты и окиси углерода. Они менее востребованы чем предыдущий вариант, но технология имеет большие перспективы для развития в будущем. На первой стадии происходит синтез из окиси или двуокиси углерода муравьинокислых солей, а затем их трансформируют в оксалаты. Далее они используются как отдельное сырье или проходят через реакцию восстановления для получения непосредственно щавелевой кислоты.
Сферы применения щавелевой кислоты
Химическое вещество имеет самую широкую область применения в производстве. Прежде всего, щавелевая кислота – востребованный реактив по многим направлениям аналитической химии. С ней связан синтез йодовода, соединений на основе хлора.
Кроме этого, щавелевую кислоту используют в гальванотехнике, чтобы в анодных ваннах осаждать покрытие из олова, алюминия и свинца, необходимые для различных конструкционных элементов. С ее помощью производится осаждение редкоземельных металлов из их растворов и других жидкостей технического типа. Способность этой кислоты растворять оксидные пленки и коррозионные наслоения на металлических поверхностях важна для включения в состав очистных средств производственного назначения.
В пчеловодстве реактив широко применяется для профилактики и лечения пчел от поражения клещом Варроа. В этом варианте щавелевую кислоту используют методами:
- Сублимации – для борьбы с клещом применяют испаритель щавелевой кислоты. Это специальный инструмент, с помощью которого насекомых обрабатывают парами вещества при определенной температуре с целью уничтожения вредителей.
- Опрыскивание – пасеки обрабатывают 2%-ным водным раствором.
Химикат в процессе изготовления чернил и лакокрасочной продукции. Щавелевая кислота используется при производстве пиротехнических веществ, моющих и дезинфицирующих средств бытового назначения, а также в металлургии и деревообработке.
Стоит отметить, что диэтиловый эфир щавелевой кислоты – это популярная противокоррозионная присадка к горюче-смазочным материалам. Она используется как средство протравливания сырья, которое в дальнейшем применяется в текстильном и кожевенном производстве.
Диметиловый эфир щавелевой кислоты востребован в косметической промышленностью в качестве хелатного компонента. Он является промежуточным продуктом в синтезе большой группы химических соединений.
В чистом виде химическое соединение в медицинской области не используется, но входит в состав лекарственных препаратов от онкологии. Щавелевая кислота помогает лечить злокачественные раковые опухоли путем их закисления, но вместе с тем никак не повреждает работу здоровых клеток организма.
Ранее мы уже упоминали о том, что этандиовая кислота встречается во многих продуктах питания растительного происхождения. Относительно ее количественного содержания в них из расчета на 100 г продукта:
- спаржа – 0,13 г;
- фасоль – 0,36 г;
- листья свеклы – 0,61 г;
- капуста – 0,1 г;
- морковь – 0,5 г;
- чеснок – 1,48 г;
- листья салата – 0,33 г;
- петрушка – 1,7 г;
- листья ревеня – 0,52 г;
- шпинат – 0,97 г.








