Серная кислота
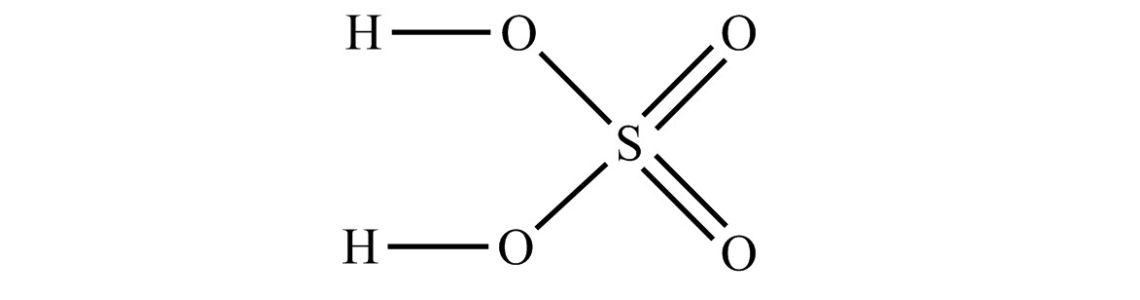

Серная кислота, формула которой H2SO4 – сильнодействующее вещество из ряда неорганических кислот с ярко выраженными химическими свойствами, которые характерны для этого класса. В чистом виде это жидкость, слегка маслянистая на вид, но прозрачная, без каких либо оттенков или яркого аромата.
Свойства серной кислоты
Степень физической плотности серной кислоты такая, что если взять ее и воду в равном объеме, то масса кислоты будет почти в 2 раза больше. Отметим, что серная кислота отлично смешивается с водой – в процессе образуются гидраты, а в окружающую среду выделяется небольшое количество тепла.
Серная кислота вступает также в химическую реакцию со всеми видами активных металлов – она всегда сопровождается выделением водорода, этот элемент замещается атомами металлов. В итоге мы получаем соли металлов, которые называются сульфатами. Не может взаимодействовать серная кислота только с благородными металлами – платиной, золотом, серебром, танталом, рутением и иридием.
Если взять реакцию взаимодействия серной кислоты с органическими химикатами, то она в процессе отделяет от них воду, и оставляет углерод в виде черного угля. Визуально подобное химическое взаимодействие выглядит, как обугливание верхних слоев любых предметов органического происхождения – как будто поджигается сахар, ткань, древесина и т. д.
Так вот, аналогичное воздействие серная кислота имеет и на человека – его слизистые оболочки и кожные покровы. Более того, из-за высокого уровня едкости серная кислота еще и опасна своими испарениями. Они способны поразить даже слизистые оболочки дыхательных путей, вызывая ряд серьезных заболеваний. Поэтому нужно соблюдать меры безопасности, чтобы исключить взаимодействие с химикатом.
Где применяется серная кислота?
В технических целях ее используют и в концентрированном, и в разбавленном виде. К примеру, для:
- синтеза сложных эфиров;
- получения этанола на основе этилена;
- в реакциях, связанных с фильтрацией и дистилляцией воды.
Серная кислота применяется в процессе изготовления волокнистых материалов синтетического происхождения, взрывчатых веществ, петард и фейерверков, лакокрасочной продукции.
В пищевой промышленности химикат используется как эмульгирующая добавка, известная под аббревиатурой Е513.
Также серной кислоте нашлось применение в:
- процессе производства синтетических моющих средств;
- добывающей отрасли – при обогащении руд, которые содержат в себе редкие химические элементы в виде иридия, урана, циркония;
- текстильной отрасли;
- нефтепереработке;
- металлообработке;
- кожевенном деле.
Используется серная кислота как электролит в процессе синтеза минеральных солей и кислот, в аккумуляторах, содержащих в себе свинец.
Но в Украине наибольшее количество производимой серной кислоты используется для изготовления минеральных удобрений. Поэтому большая часть химических предприятий, которые ее вырабатывают для продажи, строятся рядом с заводами, где и производят разные вариации минеральных удобрений на основе серой кислоты.
Процесс синтеза серной кислоты
Современная химиндустрия для получения этого химического вещества в промышленных масштабах использует контактный метод, суть которого заключается в окислении диоксида серы. Это вещество имеет вид бесцветного газа с очень резким ароматом. В итоге этой реакции окисления и образовывается серный ангидрид, или же триоксид серы – летучая бесцветная жидкость с сильным запахом, который сбивает дыхание. На следующем этапе химической реакции серный ангидрид вступает в реакцию взаимодействия с водой, итогом которой и становится получение серной кислоты.
Также, кроме контактного метода синтеза, есть еще башенный способ получения химического соединения. И состоит он в окислении диоксида серы с помощью диоксида азота и воды. В этом случае серная кислота выступает лишь побочным продуктом химического взаимодействия, и ее концентрация равна 75%.
Можно получить серную кислоту с помощью реакции взаимодействия сероводорода с сульфатами разных металлов. В этом процессе атомы металлов вытесняются, а их место занимает водород.







